Un milliardaire du monde des cryptomonnaies prévoit d'investir dans l'édition d'embryons, avec un dîner privé prévu au troisième trimestre pour les professionnels du secteur, tandis qu'une interdiction de dix ans imposée par le milieu académique fait obstacle.
TechFlow SélectionTechFlow Sélection

Un milliardaire du monde des cryptomonnaies prévoit d'investir dans l'édition d'embryons, avec un dîner privé prévu au troisième trimestre pour les professionnels du secteur, tandis qu'une interdiction de dix ans imposée par le milieu académique fait obstacle.
L'édition du génome comporte non seulement des applications médicales pratiques limitées, mais entraîne également des risques à long terme aux conséquences inconnues.
Auteurs : Luo Hua, Antonio
Récemment, Brian Armstrong, milliardaire et PDG de l'exchange de cryptomonnaies Coinbase, a déclaré qu'il était prêt à investir dans une startup américaine spécialisée dans l'édition génétique d'embryons humains.
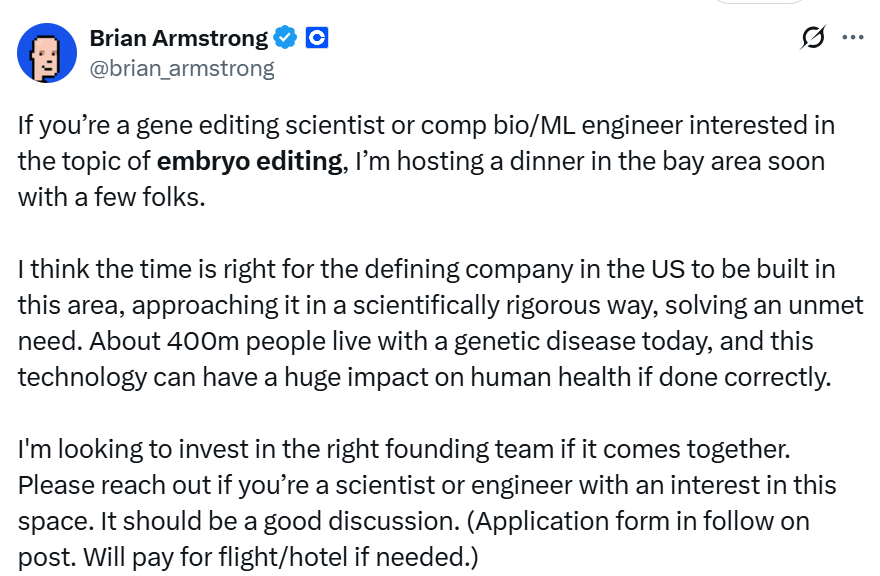
Il a publiquement recruté sur les réseaux sociaux X des scientifiques en édition génétique ou des ingénieurs en biologie computationnelle/apprentissage automatique afin de constituer une équipe fondatrice pour mener des recherches sur l’« édition embryonnaire », ciblant des besoins médicaux non satisfaits tels que les maladies génétiques. Il a invité les candidats à postuler à un dîner privé en remplissant un formulaire comprenant plusieurs questions, notamment : « Qu'est-ce de génial avez-vous créé ? »
Dans son message, il a joint une image d'un sondage du Pew Research Center datant de sept ans. Ce sondage indique que les Américains soutiennent fortement la modification génétique des bébés si elle permet de traiter des maladies, bien que la même enquête ait également révélé que la majorité s'oppose aux expérimentations sur les embryons.
Quelques semaines auparavant, plusieurs organisations du secteur biotechnologique et groupes universitaires avaient conjointement appelé à un moratoire de 10 ans sur l’édition héréditaire du génome humain, soulignant que cette technologie présente non seulement des applications médicales limitées, mais aussi des risques à long terme aux conséquences inconnues.
Ces institutions ont averti que la capacité à « programmer » des traits idéaux ou supprimer des gènes indésirables pourrait conduire à une nouvelle forme d’« eugénisme », dont les effets pourraient « modifier fondamentalement la trajectoire de l’évolution humaine ».

Jusqu'à présent, aucune entreprise américaine n'a officiellement lancé de recherche sur l'édition embryonnaire, et le gouvernement fédéral ne finance pas du tout ce type de recherche. Aux États-Unis, seuls deux centres universitaires mènent ce genre d’études : l’un dirigé par Dieter Egli, spécialiste de l’édition génétique à l’Université Columbia, et l’autre à l’Université de santé et des sciences d’Oregon.
Le financement de ces recherches est relativement limité, provenant principalement de subventions privées et de fonds universitaires. De nombreux chercheurs de ces centres affirment soutenir l'idée qu'une entreprise bien financée puisse faire avancer cette technologie. « Nous accueillons sincèrement ce type de collaboration », a déclaré Paula Amato, médecin en fertilité à l’Université de santé et des sciences d’Oregon et ancienne présidente de l’American Society for Reproductive Medicine.
Ils pensent que si un milliardaire milite en faveur de cette cause, l'interdiction actuelle sur les bébés génétiquement modifiés pourrait être levée.
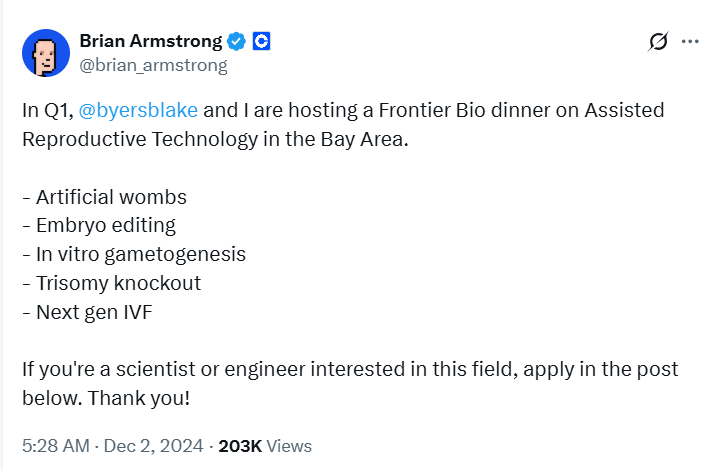
En décembre 2024, Armstrong a annoncé sur X qu’il allait rencontrer, avec l’investisseur Blake Byers, des entrepreneurs travaillant sur des projets liés à l’« utérus artificiel », à l’« édition embryonnaire » et à la « prochaine génération de fécondation in vitro ». Tous deux ont déjà cofondé NewLimit, une entreprise qui vise à prolonger la durée de vie en bonne santé grâce au reprogrammation épigénétique, ayant déjà levé près de 300 millions de dollars. Byers a déclaré que la plus grande partie du PIB mondial devrait être consacrée à la recherche sur l’« immortalité », y compris via des méthodes biotechnologiques ou le transfert du cerveau humain vers un ordinateur.
Aujourd’hui, la rencontre avec les entrepreneurs de l’« édition embryonnaire » est programmée : elle aura lieu au troisième trimestre 2025 dans la région de la baie de San Francisco. Parmi les invités figurent Stepan Jerabek, chercheur postdoctoral du laboratoire Egli, qui teste activement la technique d’édition de bases dans les embryons ; ainsi que Lucas Harrington, scientifique en édition génétique, ancien élève de Jennifer Doudna, lauréate du prix Nobel de chimie.
Harrington a indiqué que le groupe de capital-risque qu’il codirige, SciFounders, envisage également de créer une entreprise spécialisée dans l’édition embryonnaire. Dans un courriel, il a déclaré : « Nous souhaitons qu’une entreprise puisse évaluer empiriquement si l’édition embryonnaire est sûre, et nous explorons activement la création d’une société chargée de cette mission. Nous pensons qu’il faut des scientifiques et cliniciens spécialisés pour évaluer en toute sécurité cette technologie. »
Il critique par ailleurs les interdictions et moratoires imposés à cette technologie, affirmant qu’ils ne peuvent pas empêcher son utilisation, mais risquent plutôt de la pousser dans l’ombre, réduisant ainsi sa sécurité. Selon lui, certains groupes de biohackers ont déjà discrètement levé de petits montants pour faire avancer cette technologie.
En comparaison, la déclaration publique d’Armstrong sur la plateforme X reflète une attitude plus transparente. « Cette fois, cela semble sérieux, ils veulent vraiment concrétiser le projet », a déclaré Egli. Ce chercheur espère que le PDG de Coinbase financera une partie des recherches de son laboratoire : « Je pense que sa prise de parole publique est précieuse — elle permet d’évaluer la température de l’opinion, d’observer les réactions et de stimuler le débat public. »
En 2015, la Chine a été le premier pays à annoncer que des chercheurs avaient utilisé CRISPR pour modifier génétiquement des embryons humains en laboratoire, provoquant un choc mondial — on prenait conscience que modifier les caractéristiques héréditaires humaines pouvait théoriquement être très simple. En 2017, un rapport de l’État de l’Oregon aux États-Unis a affirmé avoir corrigé avec succès des mutations pathogènes dans des embryons de laboratoire issus d’ovules et de spermatozoïdes de patients.
Cependant, cette percée cachait des complications. Des chercheurs comme Egli ont découvert, grâce à des tests plus rigoureux, que la technologie CRISPR pouvait en réalité causer de graves dommages cellulaires, entraînant souvent de grandes pertes chromosomiques. Outre le phénomène de mosaïcisme (où différentes cellules subissent des éditions différenciées), cette technique d’édition ADN, apparemment précise, peut en fait produire des effets destructeurs invisibles.

Alors que le public débat âprement des questions éthiques autour des « bébés CRISPR », la communauté scientifique concentre ses efforts sur les défis fondamentaux et leurs solutions. Depuis lors, le secteur s’est tourné vers l’édition de bases, qui consiste à modifier une seule base d’ADN. Cette méthode produit moins d’effets imprévus et permet théoriquement d’introduire plusieurs variations génétiques bénéfiques chez l’embryon, plutôt qu’une seule modification. Contrairement à la méthode initiale qui coupait la double hélice, endommageant ainsi l’ADN et faisant disparaître tout le gène.
À ce jour, les thérapies d’édition génétique sont uniquement autorisées pour traiter des maladies adultes, comme la thérapie génique contre la drépanocytose, dont le coût dépasse les 2 millions de dollars. En revanche, l’édition embryonnaire pourrait être extrêmement peu coûteuse : si l’édition est réalisée très tôt dans le développement de l’embryon, toutes les cellules somatiques porteront alors la modification génétique.
Toutefois, la technologie n’est pas encore assez mature pour produire des « bébés sur mesure ». Pour atteindre cet objectif, de nombreux défis techniques restent à surmonter : concevoir précisément les systèmes d’édition, mettre en place des méthodes systématiques de détection des modifications anormales de l’ADN chez l’embryon, etc. Ce sont justement ces directions que l’entreprise envisagée par Armstrong devra explorer.
À la publication de cet article, Armstrong n’a pas répondu à la demande de commentaire de MIT Technology Review concernant ses projets, ni son entreprise Coinbase.
Bienvenue dans la communauté officielle TechFlow
Groupe Telegram :https://t.me/TechFlowDaily
Compte Twitter officiel :https://x.com/TechFlowPost
Compte Twitter anglais :https://x.com/BlockFlow_News