Desci a-t-il besoin d'un Pump ? Partir des difficultés de l'industrie pharmaceutique
TechFlow SélectionTechFlow Sélection

Desci a-t-il besoin d'un Pump ? Partir des difficultés de l'industrie pharmaceutique
Les projets DeSci actuels se concentrent principalement sur le domaine pharmaceutique, l'une des opportunités les plus accessibles pour améliorer la ressource la plus importante de l'humanité : la santé.
Source : Decentralised.co
Traduction : Yuliya, PANews
La science a toujours été le principal catalyseur du progrès humain. Pourtant, aujourd'hui, le mot « science » suscite souvent le scepticisme. Quand un titre d'actualité affirme « La science montre que… », cela provoque davantage du sarcasme qu’un véritable intérêt. Ce désenchantement croissant n’est pas sans fondement : la science est de plus en plus devenue un terme marketing, diluée par les intérêts corporatifs, s’éloignant ainsi de son objectif fondamental qui est de faire progresser la connaissance et le bien-être humains.
La science décentralisée (DeSci) se présente comme un nouveau paradigme promettant de reconstruire la recherche scientifique sur des bases plus solides. Actuellement, les projets DeSci se concentrent principalement sur le domaine pharmaceutique, l’un des fruits les plus accessibles pour améliorer la ressource la plus précieuse de l’humanité : la santé.
La crise du financement de l'innovation scientifique
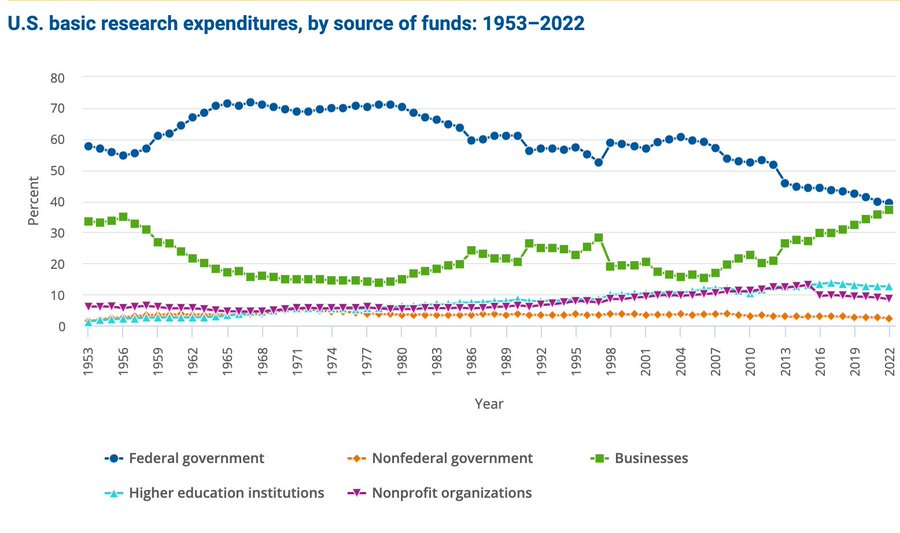
Le système traditionnel de financement scientifique est profondément défaillant. Les chercheurs académiques consacrent jusqu’à 40 % de leur temps à rédiger des demandes de subventions, avec un taux de réussite inférieur à 20 %. Alors que les fonds fédéraux diminuent, les financements privés augmentent, mais sont principalement concentrés entre les mains de grandes entreprises.
L’industrie pharmaceutique s’est transformée en un jeu à haut risque défavorable à l’innovation. Prenons une réalité brutale : sur 10 000 composés découverts, un seul parvient effectivement sur le marché. Le processus est extrêmement impitoyable. Seulement 10 % des médicaments entrant dans les essais cliniques obtiennent l’approbation de la FDA, après jusqu’à 15 ans de développement, pour un coût supérieur à 2,6 milliards de dollars par médicament réussi.
Dans les années 1990, la concentration dans l’industrie pharmaceutique semblait une bénédiction : elle apportait de l’efficacité, rationalisait la chaîne d’approvisionnement et permettait une expansion rapide de la découverte de médicaments. Mais cette machine initialement conçue comme moteur d’innovation est devenue un goulot d’étranglement, où les mêmes acteurs freinent le progrès afin de maintenir leurs monopoles, entraînant une inflation des coûts.
Dans le modèle actuel, une start-up biotechnologique passe plusieurs années à chercher un financement du NIH pour ses découvertes précoces, puis lève 15 millions de dollars lors d’un tour de financement de série A pour atteindre la phase préclinique. Si elle réussit, elle cède ses droits de propriété intellectuelle à une grande entreprise pharmaceutique, qui investit plus d’un milliard de dollars dans les essais cliniques et la commercialisation.
C’est là que les incitations se déforment. Les grands groupes pharmaceutiques ne se concentrent plus sur des thérapies radicalement nouvelles, mais maîtrisent un jeu plus lucratif : la manipulation des brevets. Leur stratégie est simple : lorsque le brevet d’un médicament très rentable arrive à expiration, ils déposent des dizaines de brevets secondaires sur des modifications mineures — un nouveau mode d’administration, une formulation légèrement modifiée, voire simplement une nouvelle indication pour le même médicament.
Prenons l’exemple du médicament anti-inflammatoire Humira d’AbbVie. Pendant des années, Humira a été l’un des médicaments les plus vendus au monde, générant plus de 20 milliards de dollars de revenus annuels. Son brevet initial est arrivé à échéance en 2016, mais AbbVie a déposé plus de 100 brevets supplémentaires pour bloquer la concurrence des génériques. Ces manœuvres juridiques ont retardé l’arrivée de substituts abordables sur le marché, faisant payer aux patients et aux systèmes de santé des milliards de dollars.
Lors d’un récent débat DeSci entre Tarun Chitra et benjels, la question du ralentissement de l’innovation pharmaceutique a été soulevée, avec référence à la loi d’Eroom (l’inverse de la loi de Moore).
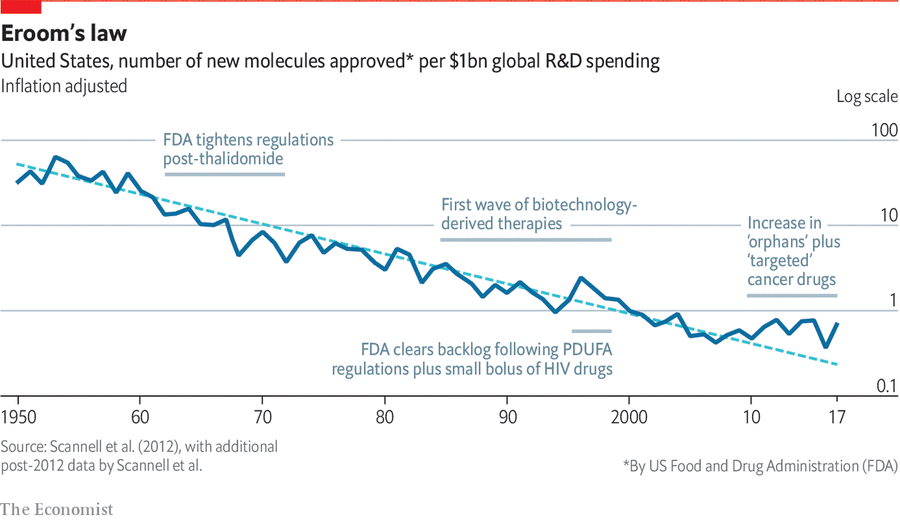
Ces pratiques reflètent un problème plus vaste : l’innovation est capturée par la quête de profit. Les entreprises pharmaceutiques investissent leurs ressources dans l’ajustement mineur de médicaments existants — modifications chimiques minimes ou recherche de nouveaux mécanismes d’administration — non pas parce que cela apporte de réels bénéfices pour la santé, mais parce que cela permet d’obtenir de nouveaux brevets et de prolonger la période de rentabilité.
Une science sur une meilleure trajectoire
Entre-temps, une communauté mondiale de chercheurs talentueux et créatifs reste exclue de ce processus. Les jeunes chercheurs sont limités par des financements restreints, la bureaucratie et une culture du « publie ou péris » qui valorise le sensationnel plutôt que les recherches significatives. Résultat : les maladies rares, les maladies tropicales négligées et les recherches exploratoires précoces souffrent cruellement de sous-financement.
La DeSci est essentiellement un mécanisme de coordination. Elle rassemble le capital humain mondial — biologistes, chimistes, chercheurs — leur permettant de synthétiser, tester et itérer sans dépendre des institutions traditionnelles. Le modèle de financement est également repensé. Les organisations autonomes décentralisées (DAO) et les incitations par jetons remplacent les subventions gouvernementales ou le parrainage d’entreprise, démocratisant ainsi l’accès au capital.
La chaîne d’approvisionnement pharmaceutique traditionnelle est un processus rigide et isolé, dominé par quelques intermédiaires. Elle suit généralement un chemin linéaire : génération centralisée de données, découverte en laboratoires fermés, essais coûteux, fabrication exclusive et distribution restreinte. Chaque étape est optimisée pour le profit, pas pour l’accessibilité ou la collaboration.
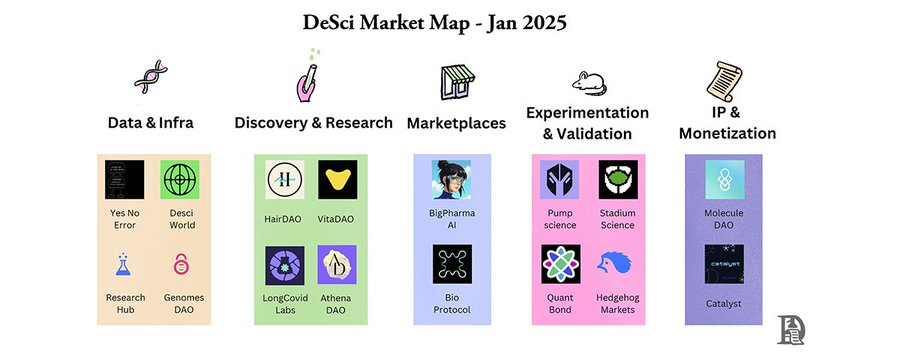
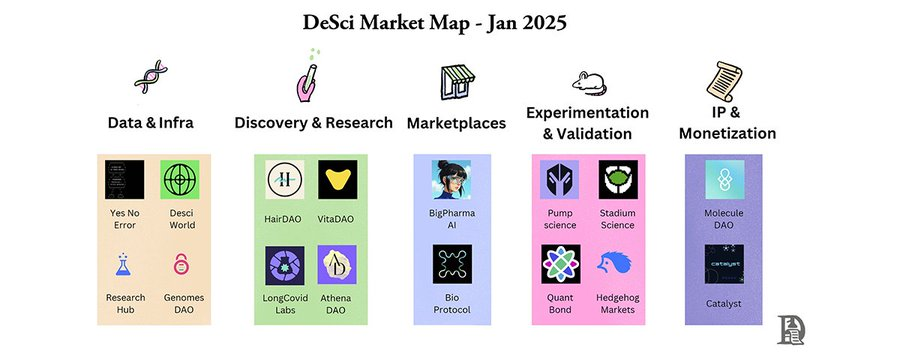
À l’inverse, la DeSci introduit une chaîne de collaboration ouverte, repensant chaque étape pour démocratiser la participation et accélérer l’innovation. Cela se manifeste principalement par les aspects suivants :
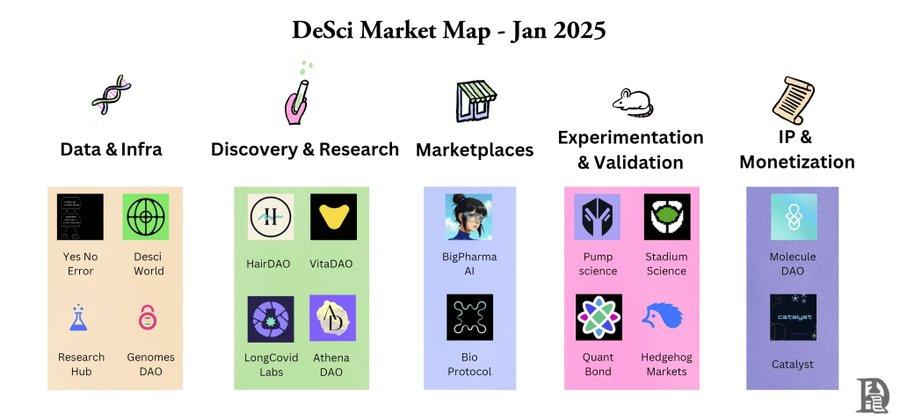
1. Données et infrastructure
Modèle traditionnel : les données sont propriétaires, fragmentées et souvent inaccessibles. Les instituts de recherche et les entreprises pharmaceutiques accumulent des jeux de données pour préserver leur avantage concurrentiel.
Modèle DeSci : les plateformes regroupent et démocratisent l’accès aux données scientifiques, créant ainsi les bases d’une collaboration transparente.
Exemple : yesnoerror utilise l’IA pour détecter les erreurs mathématiques dans les articles publiés, renforçant la reproductibilité et la crédibilité de la recherche.
2. Découverte et recherche
Modèle traditionnel : la découverte a lieu dans des laboratoires académiques ou industriels fermés, limitée par les priorités de financement et les questions de propriété intellectuelle.
Modèle DeSci : les DAO financent directement les recherches précoces, permettant aux scientifiques d’explorer des idées novatrices sans la bureaucratie institutionnelle.
Exemple : VitaDAO a levé des millions de dollars pour financer des recherches sur la longévité, soutenant des projets sur le vieillissement cellulaire et la découverte de médicaments qui auraient autrement du mal à obtenir des fonds. HairDAO est un collectif de chercheurs et de patients qui documente les expériences de traitement de la perte de cheveux avec différents composés.
3. Marchés
Modèle traditionnel : contrôlé par des intermédiaires. Les chercheurs dépendent des éditeurs traditionnels, des conférences et des réseaux pour partager leurs découvertes et obtenir des ressources.
Modèle DeSci : les marchés décentralisés connectent mondialement chercheurs, financeurs et outils.
Exemple : Bio Protocol offre aux chercheurs une plateforme pour créer des BioDAO — ces DAO visent la recherche de nouveaux composés, assurent un financement continu pour les actifs biotechnologiques nouvellement créés, et offrent un marché liquide pour les IP tokenisées. Comparé au domaine des agents IA, Bio peut être vu comme les Virtuals du monde DeSci.
Big Pharmai, homologue d’ai16z, lance sur Daos.fun des investissements dans des jetons DeSci. Ses actifs sous gestion dépassent déjà 1 million de dollars, et il prévoit de lancer son propre cadre d’agents Bio.
4. Expérimentation et validation
Modèle traditionnel : les essais précliniques et cliniques sont coûteux, généralement réservés aux grandes entreprises pharmaceutiques. La transparence est minimale, les échecs sont souvent dissimulés.
Modèle DeSci : les plateformes décentralisent les essais, permettant une participation mondiale et un financement via des jetons.
Exemple : Pump Science utilise des courbes de liaison pour financer par crowdfunding des expériences sur la longévité, faisant passer des composés des tests sur vers à ceux sur mouches, puis rats, avant commercialisation.
Des chercheurs médicaux peuvent soumettre des propositions de recherche sur Pump Science, la plateforme aide à tester ces médicaments sur des vers, et transmet les résultats expérimentaux en temps réel à l’interface. Les utilisateurs peuvent spéculer sur les jetons représentant ces médicaments. Deux jetons populaires, Rif (rifampicine) et URO (urolithine A), sont testés sur des vers ; si un allongement de la durée de vie est constaté, ces composés passeront à la phase commerciale, et les détenteurs partageront les profits.
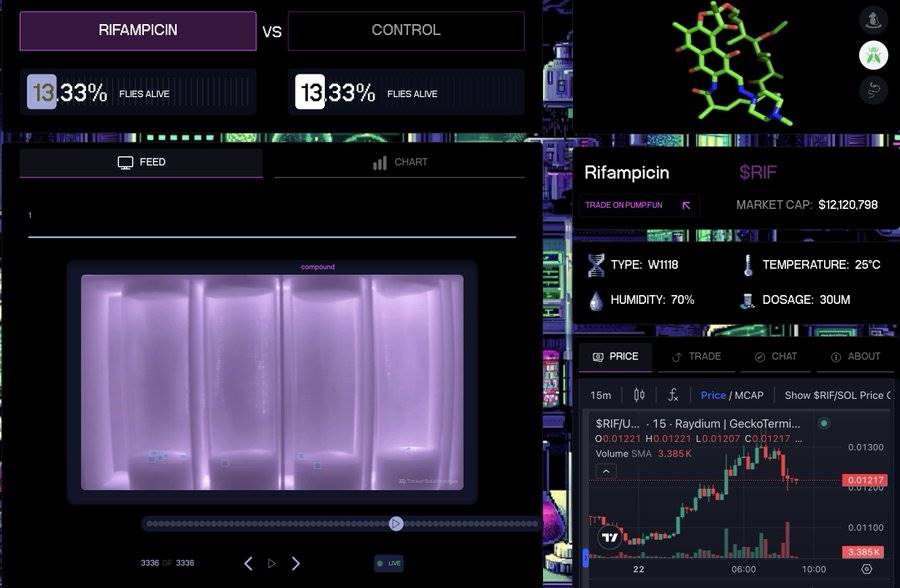
Les résultats de ces essais sont enregistrés et diffusés en direct sur Pump.science
5. Propriété intellectuelle et monétisation
Modèle traditionnel : la propriété intellectuelle est verrouillée dans des monopoles brevetés, créant des obstacles à l’innovation et gonflant les prix des médicaments. Déposer un brevet pour un nouveau composé est coûteux et extrêmement complexe.
Modèle DeSci : les protocoles tokenisent les IP, permettant aux chercheurs de partager et de monétiser leurs découvertes de manière transparente.
- Exemple : le cadre IP de Molecule permet aux chercheurs de financer leurs projets en divisant les droits de propriété intellectuelle en NFT et jetons, alignant ainsi les incitations entre scientifiques et financeurs. Toutefois, ce modèle en est encore à ses débuts. Peu de chercheurs ont testé la tokenisation de leurs IP, et il est difficile d’estimer comment les profits seront distribués aux détenteurs lors de la commercialisation. En outre, pour garantir une protection adéquate des IP, les chercheurs devront probablement continuer à déposer leurs brevets auprès des institutions gouvernementales traditionnelles.
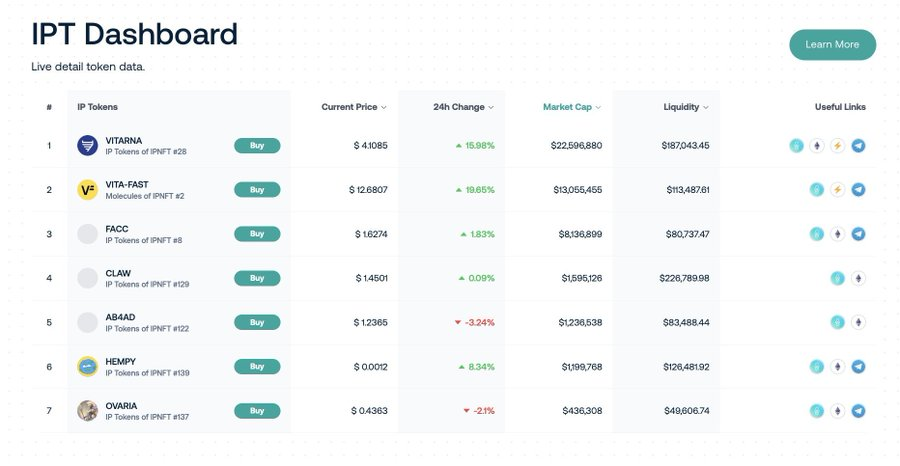
Les BioDAO détiennent via le cadre Molecule plus de 33 millions de dollars d’IPT tokenisés
Le défi de la responsabilité
Les DAO rencontrent des difficultés pour coordonner des tâches complexes et assurer une responsabilité durable — peu d’entre eux ont fait preuve de succès soutenu dans la gestion de projets à long terme. La DeSci fait face à un défi encore plus grand : elle exige que les chercheurs collaborent sur des problèmes complexes, respectent des délais de recherche et maintiennent la rigueur scientifique, le tout sans supervision institutionnelle traditionnelle.
La science traditionnelle, malgré ses défauts, dispose de mécanismes d’évaluation par les pairs et de contrôle qualité. La DeSci doit soit améliorer ces systèmes, soit développer des cadres de responsabilité entièrement nouveaux. Étant donné les risques élevés liés à la recherche médicale, ce défi est particulièrement sévère. L’échec d’un projet NFT peut entraîner une perte d’argent, mais un essai médical mal conduit peut mettre des vies en danger.
Les critiques considèrent que la DeSci n’est qu’un comportement spéculatif — rien de plus qu’un jeu de trading. Cette affirmation n’est pas totalement fausse. L’histoire montre que les nouvelles technologies traversent souvent une phase de tâtonnement avant de connaître un succès décisif et de capter l’imagination du public. Tout comme les agents IA ont gagné en notoriété grâce à des projets comme aixbt, la DeSci pourrait aussi avoir besoin d’un moment déterminant pour changer la perception.
L’avenir ne suivra peut-être pas exactement la vision des partisans de la DeSci. Peut-être ne s’agit-il pas de remplacer complètement les institutions traditionnelles, mais de créer des systèmes parallèles qui stimulent l’innovation par la concurrence. Ou alors, il pourrait s’agir de trouver des niches spécifiques — comme la recherche sur les maladies rares — là où le modèle traditionnel a échoué.
Imaginons un monde où les esprits brillants, libres des contraintes géographiques et budgétaires, s’attaquent aux plus grands défis médicaux de l’humanité — une percée réalisée dans un laboratoire chinois pouvant être instantanément validée à Singapour et industrialisée à São Paulo.
Les pionniers construisent cet avenir pas à pas. Prenons l’exemple de Bryan Johnson — ce biohackeur indépendant expérimente des médicaments hors AMM et des thérapies non conventionnelles. Bien que sa méthode puisse inquiéter les traditionalistes, il incarne l’esprit de la DeSci : l’expérimentation prime sur les gardiens.

Bienvenue dans la communauté officielle TechFlow
Groupe Telegram :https://t.me/TechFlowDaily
Compte Twitter officiel :https://x.com/TechFlowPost
Compte Twitter anglais :https://x.com/BlockFlow_News
















