Pourquoi Binance investit dans BIO Protocol ? Découvrez en un article la nouvelle narration DeSci
TechFlow SélectionTechFlow Sélection

Pourquoi Binance investit dans BIO Protocol ? Découvrez en un article la nouvelle narration DeSci
Cet article vous aide à comprendre pourquoi Binance investit dans BIO Protocol. Il examine l'évolution du financement de la recherche scientifique, la structure actuelle des institutions scientifiques existantes, et la manière dont les technologies Web3, ainsi que la narration actuelle autour de DeSci, transforment le financement et l'organisation de la recherche scientifique.
Auteurs originaux : Elliot Hershberg et Jocelynn Pearl
Traduction : LlamaC
 (Portfolio : Burning Man 2016, à propos de Tomo : illustrateur de la fondation eth)
(Portfolio : Burning Man 2016, à propos de Tomo : illustrateur de la fondation eth)
« Recommandation : Cet article vous aide à comprendre pourquoi Binance a investi dans BIO Protocol. Il explore l’évolution du financement de la recherche scientifique, la structure des institutions scientifiques existantes, ainsi que la manière dont les technologies Web3 et la narration actuelle de DeSci transforment le financement et l’organisation de la science. »
Contenu principal👇
La science est l'outil fondamental du progrès humain.
C’est un système que nous avons construit afin d’élaborer des explications détaillées et robustes sur la réalité objective. Ces types d’explications exigent des modèles cohérents capables d’interpréter les observations empiriques. La seule méthode pour y parvenir consiste à mener des travaux expérimentaux et théoriques rigoureux, garantissant que chaque détail de l’explication joue un rôle fonctionnel et reste étroitement lié à la réalité objective. Ce type d’explication constitue précisément ce qui nous a fait passer des mythes à la physique, des cavernes aux gratte-ciels. Le physicien David Deutsch considère cela comme l'idée centrale de la révolution scientifique : « Depuis lors, notre compréhension du monde physique et notre capacité à l'adapter à nos désirs n’ont cessé de croître. »
La lumière directrice de la découverte scientifique est l’une de nos ressources les plus précieuses, qu’il convient de gérer avec soin. Outre le développement de nouvelles explications, nous avons mis en place un système humain complexe transformant les connaissances nouvelles en inventions qui font avancer le monde moderne. Il est crucial d’étudier et d’améliorer ce système — ce qui implique d’interagir avec une multitude de systèmes humains complexes. Comme l’a souligné le visionnaire Vannevar Bush : « Nous avons besoin que législateurs, tribunaux et public comprennent mieux cette affaire complexe dans son ensemble. Les inventions ne manqueront pas ; les vrais inventeurs sont incapables de s’empêcher d’inventer. Mais nous voulons davantage d’inventions réussies, et pour cela, il faut une meilleure compréhension. »
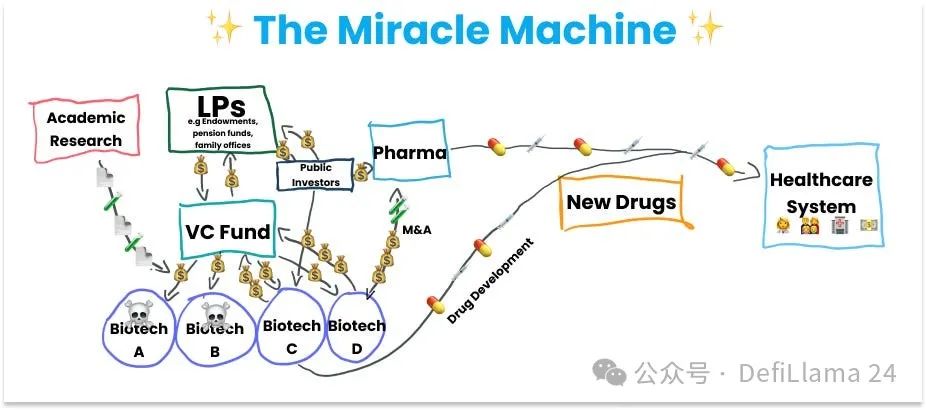
Guidé par la mission d’accélérer le progrès scientifique, Vannevar Bush a mené les efforts d’extension du système américain de financement de la recherche jusqu’à l’échelle actuelle. Ce système puissant est ce que le scientifique et ancien directeur du Bureau de politique scientifique et technologique, Eric Lander, appelle la « machine à miracles ».
 Machine à miracles ; créée avec Midjourney
Machine à miracles ; créée avec Midjourney
Nos efforts systématiques de financement de la science fondamentale ont abouti à des percées telles que l’internet, l’intelligence artificielle, les immunothérapies contre le cancer ou encore CRISPR, la technologie d’édition génétique. Bien que les résultats obtenus jusqu’ici soient miraculeux, cette machine ne fonctionne pas seule : entretenir ce système est absolument essentiel.
Pourtant, au fil du temps, nous sommes devenus complaisants dans l’entretien de cette machine.
Lander a forgé ce terme tout en plaidant passionnément pour une augmentation du budget fédéral de recherche, alors même que ces dernières années, les budgets de recherche ont diminué. Depuis 2003, le budget ajusté à l'inflation des instituts nationaux de santé (NIH), principale agence fédérale de recherche biomédicale, a baissé de près de 25 %. Le défi du financement scientifique dépasse largement la simple revendication d’un budget plus important. Nos mécanismes concrets de financement sont devenus de plus en plus rigides, inefficaces, et pilotés par le consensus. Une étude gouvernementale américaine estime que les professeurs passent désormais environ 40 % de leur temps de recherche à naviguer dans un labyrinthe bureaucratique nécessaire pour financer leurs laboratoires. Dans une autre enquête alarmante, 78 % des chercheurs ont déclaré qu’ils changeraient « radicalement » leurs plans de recherche s’ils disposaient de fonds sans restriction. Les jeunes scientifiques rencontrent également un goulot d’étranglement sévère pour obtenir des financements dès le début de leur carrière, précisément à une période qui pourrait être la plus productive et novatrice de toute leur vie.
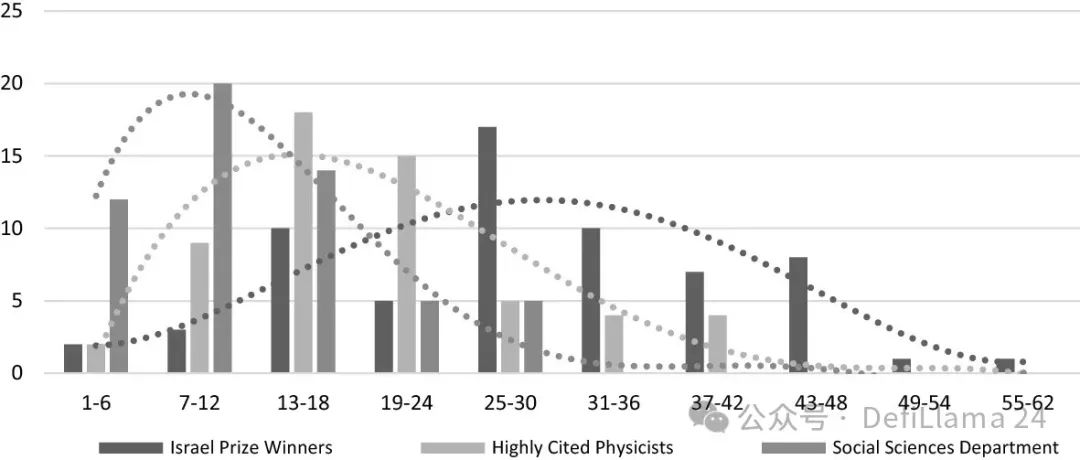 Yair & Goldstein, 2019. Figure 2 : Distribution de l’âge professionnel correspondant à l’année miracle (ou année de publication maximale) dans trois petites études
Yair & Goldstein, 2019. Figure 2 : Distribution de l’âge professionnel correspondant à l’année miracle (ou année de publication maximale) dans trois petites études
Au-delà du financement des laboratoires, d’importants goulets d’étranglement structurels entravent la transformation des découvertes scientifiques en nouveaux médicaments et produits. C’est ce que l’ancien directeur des NIH, Elias Zerhouni, appelait la « vallée de la mort ». Ces dernières années, la création d’entreprises biotechnologiques a ralenti. Le médecin-scientifique Eric Topol a récemment souligné que malgré nos avancées profondes dans la compréhension du génome humain, ces connaissances n’ont pas encore été appliquées concrètement en clinique.
Tout optimiste et partisan du progrès humain devrait considérer la santé et l’efficacité de notre « machine à miracles » comme une priorité absolue, alors que nous sommes clairement loin de réaliser notre plein potentiel.
Alors, que pouvons-nous faire ?
Les défis et les inefficacités ouvrent la voie à de nouvelles opportunités. Ces dernières années, les innovations dans les mécanismes de financement de la recherche ont explosé. La métascience — l’étude de la science elle-même — est devenue une discipline appliquée. La future « machine à miracles » sera-t-elle une version modernisée de notre système actuel, ou quelque chose de totalement nouveau ? Où et comment se produira la prochaine vague de progrès scientifique ? Ce sont là des questions fondamentales pour presque tous les types d’innovation. Pour reprendre R. Buckminster Fuller : « On ne change jamais rien en luttant contre la réalité existante. Pour changer quelque chose, construisez un nouveau modèle qui rende l’ancien obsolète. »
Lorsqu’on analyse des systèmes humains complexes comportant plusieurs couches d’incitations, suivre l’argent est souvent un conseil étonnamment judicieux.
All the President's Men | Follow The Money Scene | Warner Bros. Entertainment
https://youtu.be/QodGxD19_as
Notre objectif ici est de mieux comprendre comment nous alimentons actuellement notre machine à miracles. Comment finançons-nous réellement l’innovation scientifique et sa commercialisation ? À partir de là, nous examinerons les idées, technologies et projets visant à transformer ce processus.
Plongeons-nous dans certaines innovations récentes du financement de la recherche, allant du capital privé aux cryptomonnaies, en passant par la création d’institutions entièrement nouvelles consacrées à l’exploration des domaines inconnus de notre compréhension scientifique.
Nous explorerons :
- Une vue d’ensemble macro du financement scientifique actuel
- Un cas d’usage phare du Web3
- Plus de gaz, plus vite financé
- Adopter pleinement Bucky (construire depuis zéro)
Vue d’ensemble macro du financement scientifique actuel
Comment est concrètement construite la machine à miracles actuelle ?
Presque toutes les disciplines scientifiques se divisent approximativement en trois catégories d’organisations :
- Institutions académiques (universités, instituts à but non lucratif, etc.)
- Start-ups
- Entreprises (sociétés établies possédant des laboratoires de R&D)
Illustrons cela en observant le fonctionnement dans le domaine biomédical. Les Instituts Nationaux de Santé (NIH) disposent d’un budget annuel d’environ 45 milliards de dollars, ce qui en fait la principale source de financement de la recherche biomédicale. D'autres organismes, comme la Fondation Nationale pour la Science (NSF), avec un budget annuel d’environ 8 milliards de dollars, sont également des bailleurs importants. Ces grandes agences gouvernementales attribuent des fonds via divers mécanismes de subvention aux chercheurs principaux (PIs) qui en font la demande. Les PIs sont généralement des professeurs dans des universités ou des facultés de médecine, chargés de gérer un laboratoire. Les travaux de recherche sont réalisés par des étudiants diplômés, des post-doctorants temporaires et quelques professionnels, tandis que le PI joue un rôle de gestionnaire.

Cette structure hiérarchique de financement et d’organisation n’est pas la seule façon possible de mener des recherches en laboratoire. Le chimiste et microbiologiste éminent Louis Pasteur (dont le procédé de pasteurisation porte le nom) a personnellement réalisé avec minutie de nombreuses expériences, assisté seulement par ses aides expérimentateurs (comme indiqué ci-dessus). C’était en fait une partie essentielle de sa démarche : il s’entraînait à garder un « esprit préparé », capable de remarquer même les résultats les plus subtils dans ses expériences. Aujourd’hui, la blague courante selon laquelle « Attention quand le chercheur principal entre au laboratoire » reflète bien le fait que leurs compétences pratiques ont souvent disparu.
Emily Noël a endommagé du matériel de laboratoire lors d'une manipulation en raison d'une force excessive.
https://x.com/noelresearchlab/status/1171376608437047296
Il est difficile de dater exactement le passage au système moderne de laboratoire, mais la Seconde Guerre mondiale fut un tournant décisif. Vu l’importance du Projet Manhattan dans l’effort de guerre, le financement scientifique a connu un changement majeur : il ne s’agissait plus simplement de soutenir la quête de savoir — le financement scientifique avait désormais un impact direct sur la sécurité nationale et la croissance économique. Ces idées furent parfaitement exprimées dans le rapport de 1945 de Vannevar Bush intitulé *Science — La frontière infinie*.
Dans les années qui ont suivi, de nombreuses institutions scientifiques et biomédicales actuelles ont vu le jour. Depuis la Seconde Guerre mondiale, le nombre d’écoles de médecine aux États-Unis a doublé. Entre 1945 et 1965, les effectifs professoraux ont augmenté de 400 %. La science n’était plus une activité intellectuelle solitaire, mais de plus en plus une entreprise collective financée par des subventions publiques. On parle souvent de la « bureaucratisation croissante » de la science.
Ainsi, la première grande roue de la machine à miracles est constituée des laboratoires de recherche financés par l’État.
Ces laboratoires ont pour mission de construire les explications fondamentales du monde, rendant ainsi possible leur transformation. La commercialisation de la science se fait par la création d’entreprises dérivées centrées sur des propriétés intellectuelles (IP) ayant un potentiel de transformation. Ces spin-offs sont financés par des sociétés de capital-risque (VC), elles-mêmes financées principalement par des partenaires limités (LP). Les LP sont des institutions telles que les fonds de dotation universitaires, les caisses de retraite ou les bureaux familiaux.
C’est la deuxième grande roue de la machine à miracles : les start-ups et entreprises dérivées universitaires soutenues par le capital privé.
Les start-ups biotech se concentrent principalement sur l’élargissement et le développement de la science initiale autour de laquelle elles ont été créées, et sur le processus ardu et long d’obtention de l’approbation de nouveaux médicaments. Ce processus ne s’arrête pas à l’approbation. Les médicaments doivent être produits, commercialisés et vendus mondialement. Cette phase est assurée par les grandes sociétés pharmaceutiques, dont beaucoup sont des multinationales existant depuis plus d’un siècle, parfois même antérieures à la création de la FDA, l’agence responsable de l’approbation des médicaments. Ces entreprises ne développent généralement pas elles-mêmes les médicaments, mais achètent des actifs aux sociétés biotech, souvent en rachetant l’entreprise entière.
Les grandes entreprises pharmaceutiques à forte intensité de R&D constituent la troisième grande roue de notre machine à miracles actuelle.
Cette machine a effectivement produit des miracles.
L’histoire de Genentech n’est qu’un exemple. Des travaux académiques pionniers à l’université Stanford ont été transférés vers une entreprise soutenue par du capital-risque. Cette entreprise a réussi à utiliser l’ingénierie génétique pour transformer des cellules bactériennes en minuscines usines de production d’insuline — résolvant ainsi grandement une pénurie critique d’un médicament vital. En 2009, Genentech a fusionné avec le géant pharmaceutique suisse Roche dans une transaction de 47 milliards de dollars, promettant une industrialisation mondiale.
L’histoire ne s’arrête pas là. Des percées telles que les thérapies cellulaires ou l’édition génétique CRISPR sont encore en cours de transition des laboratoires académiques vers des applications cliniques. Les laboratoires académiques continuent de développer de nouvelles théories et modèles, et de nouvelles entreprises continuent d’émerger et d’être financées autour des avancées les plus prometteuses. L’industrie pharmaceutique reste le principal acheteur et distributeur mondial. Ce système a atteint un certain équilibre stable entre ses différents acteurs.
Bien que la machine à miracles ait amélioré notre monde, des défis systémiques sont apparus au fil du temps. Nous présentons cette vue d’ensemble du système actuel afin de faciliter la compréhension de certains de ses problèmes, et de fournir un contexte pour appréhender les nouveaux projets qui cherchent à les résoudre.
De grandes agences de financement comme les NIH sont devenues, avec le temps, de plus en plus bureaucratisées, et ont naturellement tendance à privilégier des projets plus conservateurs et progressifs. Nous sommes assez sûrs que personne ne pense vraiment que les scientifiques devraient passer jusqu’à 40 % de leur temps à remplir des paperasses gouvernementales fastidieuses. Alors que le processus de financement devient de plus en plus complexe et piloté par comités, il devient de plus en plus difficile de soutenir de nouvelles directions de recherche prometteuses.
Les NIH montrent aussi un intérêt croissant pour les projets de « grande science », qui organisent de grands groupes de recherche pour des projets trop ambitieux pour un seul laboratoire. Bien que cela semble important en théorie, les résultats de ces projets sont mitigés, et ils consomment des ressources qui auraient pu être utilisées pour financer des laboratoires axés sur la découverte fondamentale. Comme l’a dit le biologiste de Berkeley Michael Eisen : « Les grands projets en biologie ne sont pas une bonne nouvelle pour la science de découverte individuelle. Ironiquement et tragiquement, ils deviennent la menace la plus sérieuse pour la survie continue de celle-ci. »
Des changements structurels massifs dans le financement public de la recherche ont façonné et limité les types de questions scientifiques que les chercheurs peuvent aborder. Le relais entre universités et start-ups est aussi devenu plus complexe. Lors de la phase de transformation, les conditions imposées par les entreprises dérivées universitaires varient fortement, et dans certains cas, compromettent l’entreprise avant même son démarrage. Les universités ont un fort incitatif à protéger strictement leur propriété intellectuelle, ce qui peut conduire à des conditions plus défavorables pour les scientifiques, voire à des termes si désavantageux que les investisseurs perdent tout intérêt à financer ces efforts de transformation.
Les agences gouvernementales ne sont pas les seules à présenter des lacunes de financement. Les capitalistes-risqueurs ont eux aussi des limitations inhérentes quant aux projets dans lesquels ils peuvent investir — une entreprise doit avoir le potentiel de générer une sortie massive de plus d’un milliard de dollars pour que le modèle financier soit attrayant. Toutes les technologies ou biens publics ne peuvent pas produire un tel retour, surtout dans les délais restreints des investisseurs. Seule une petite fraction de la population a la possibilité, en tant qu’investisseur accrédité, de participer à ces investissements privés et d’accéder à une véritable richesse, ce qui accentue encore les inégalités.
Les entreprises pharmaceutiques sont également limitées par leur structure financière et leurs incitations. Leur motivation explicite est de développer ou d’acquérir les médicaments les plus rentables, tout en minimisant les coûts de R&D. Cela déforme de façon sous-optimale l’ensemble du pipeline, avec des conséquences réelles : « Malgré des besoins médicaux non satisfaits importants et un fardeau élevé de maladies, presque aucun produit n’est en développement pour traiter la résistance aux antimicrobiens, la tuberculose ou la dépendance aux opioïdes. En revanche, de nombreux nouveaux produits sont des versions légèrement modifiées de médicaments existants. »
Où devrions-nous donc chercher de nouvelles idées et méthodes ?
Il est peu probable que des solutions radicales viennent des dirigeants de nos institutions actuelles, qui ont tout intérêt à perpétuer le système existant. Une direction intéressante pour trouver de nouvelles idées est d’explorer les projets secondaires menés par des scientifiques innovants. Comme l’a dit Paul Graham à propos des meilleures idées de start-up : « Les meilleures idées doivent presque toujours commencer comme des projets secondaires, parce qu’elles sont toujours si différentes que votre esprit conscient les rejette comme des idées d’entreprise. »
En adoptant cette approche, il est difficile d’ignorer l’expansion progressive de la communauté de la science décentralisée (DeSci).
Un cas d’usage phare du Web3
Personnellement, j’étais initialement très sceptique vis-à-vis du web3. En tant que scientifique et ingénieur, l’un de mes centres d’intérêt principaux est de construire des outils de pointe pour les scientifiques en exploitant la puissance du web2 — bases de données centralisées efficaces, serveurs rapides, navigateurs modernes performants. Des analyses techniques comme celles de Moxie Marlinspike sur les premières impressions du web3 ont longtemps fondé ma pensée sur ce domaine.
Mais au fil du temps, je suis devenu un optimiste prudent — ironiquement, précisément au moment où le marché des cryptomonnaies s’effondrait et que le scepticisme envers le web3 croissait. Pourquoi ? Lorsque je discutais avec des personnes intelligentes comme Packy, Jocelynn ou certains fondateurs leaders du secteur, je me suis enthousiasmé à l’idée des domaines dans lesquels ce nouvel ensemble de protocoles, outils et concepts pourrait exceller. Nous assistons à des expériences sociales importantes, tentant de créer de nouveaux modes de collaboration et d’organisation. Ayant une expérience directe dans la science académique, je sais que nos institutions de recherche pourraient bénéficier d’un changement de statu quo.
Les lecteurs de Not Boring connaissent probablement la récente controverse autour des cas d’usage du Web3 dans laquelle notre intrépide leader Packy s’est retrouvé impliqué. Un avantage tangible du web3 est qu’il offre un nouvel ensemble d’outils pour créer des instruments financiers. Comme l’a souligné Michael Nielsen : « De nouveaux instruments financiers peuvent à leur tour servir à créer de nouveaux marchés et permettre de nouvelles formes de comportement humain collectif. »
Et si l’un des cas d’usage phares de cette nouvelle pile technologique était d’améliorer radicalement le processus de financement de la recherche ?
Comme nous l’avons souligné jusqu’ici, le financement de la recherche se divisait traditionnellement grossièrement en deux catégories : financement public ou privé. Une fois que les investisseurs en cryptomonnaies ont accumulé d’immenses richesses, une troisième catégorie de financement est apparue, et beaucoup de ces nouveaux investisseurs souhaitent utiliser leur argent à des fins bénéfiques.
Ce point mérite une brève réflexion. L’essor des cryptomonnaies a créé un nouveau type de milliardaires, principalement des personnes prêtes à être les premiers adoptants d’un système financier entièrement nouveau. Comme Tyler Cowen l’a argumenté, cela pourrait transformer le monde de la philanthropie, car cette nouvelle élite technologique pourrait s’intéresser davantage à des « projets indépendants inhabituels ». Nous voyons déjà ce phénomène à l’œuvre : Vitalik Buterin et Brian Armstrong ont tous deux effectué de gros investissements dans des projets liés à la longévité.
Cette différence ne se limite pas à l’émergence d’un groupe plus jeune et plus technophile d’investisseurs et de philanthropes. Les technologies web3 sont utilisées pour renforcer le financement de projets scientifiques novateurs et inhabituels. Aujourd’hui, de nouveaux mécanismes de financement, comme les ventes de jetons ou la collecte de fonds soutenue par des cryptomonnaies, introduisent une manière entièrement nouvelle de financer des projets.
Le financement participatif a toujours été difficile pour la recherche scientifique, mais la collecte de fonds en cryptomonnaies pourrait changer cela. Une série de nouveaux protocoles ouverts et d’outils sont apparus, visant à élargir le financement des biens publics. Gitcoin en est un exemple : une organisation dédiée à la construction et au financement de biens publics. À chaque trimestre, ils lancent une campagne de financement participatif soutenue par de grands donateurs comme Vitalik Buterin. L’innovation notable ici est l’utilisation du matching quadratique — signifiant que le nombre de donateurs influence davantage le montant apparié que le montant des dons eux-mêmes. Lors du dernier cycle GR15, la science décentralisée (DeSci) a été classée parmi les quatre catégories d’impact, soulignant une fois de plus l’intérêt croissant du secteur web3 pour la recherche scientifique.
Cycle de subventions GitcoinGR15
https://x.com/umarkhaneth/status/1575147449752207360
Le volet DeSci a reçu des dons de 2 309 contributeurs uniques, soutenant 83 projets pour un total de 567 983 dollars. Un groupe intéressant de grands financeurs a fourni les fonds appariés ; parmi eux figuraient Vitalik Buterin (cofondateur d’Ethereum), Stefan George (cofondateur et CTO de Gnosis), Protocol Labs… et même Springer Nature Group.

La communauté scientifique emprunte une autre innovation blockchain : les organisations autonomes décentralisées (DAOs).
Comme Packy l’a déjà décrit, les DAO sont une innovation dans la gouvernance web3. Elles « fonctionnent sur la blockchain, donnant le pouvoir décisionnel aux parties prenantes plutôt qu’aux cadres ou aux membres du conseil d’administration ». Elles sont « autonomes » car elles reposent sur des protocoles logiciels enregistrés sur une blockchain publiquement accessible, « déclenchant des actions automatiquement si certaines conditions sont remplies, sans intervention humaine. »
À l’instar de Gitcoin et du financement quadratique, l’un des cas d’usage les plus excitants des DAO est d’accélérer la création et le financement de communautés scientifiques. Au cours de l’année dernière, les DAO scientifiques ont connu une explosion comparable à l’explosion cambrienne. Voici un aperçu de certains DAO et projets dans ce domaine :
 UltraRare Bio a compilé et mis à jour cet aperçu du paysage DeSci le 13 octobre 2022
UltraRare Bio a compilé et mis à jour cet aperçu du paysage DeSci le 13 octobre 2022
Si nous considérons la science traditionnelle comme une approche « descendante » se déroulant dans des centres universitaires établis et hautement centralisés, les DAO scientifiques illustrent une tendance ascendante vers une science « ascendante ». Plusieurs communautés dans ce domaine se forment lorsque des groupes adoptent un objectif commun — par exemple, faire avancer la recherche en agriculture ou contre la perte de cheveux. Ce ne sont pas simplement des forums de discussion comme Reddit ; la plupart des DAO incluent des groupes de travail spécialisés, mélangeant souvent experts et scientifiques amateurs, qui s’attaquent à des tâches comme réaliser de nouvelles synthèses bibliographiques dans leur domaine ou évaluer des projets pour financement.
L’une des promesses initiales de DeSci est la démocratisation de l’accès au financement ; fondamentalement, des recherches auparavant impossibles à financer obtiennent maintenant des fonds. Mais est-ce vrai pour des projets financés par des communautés comme le groupe Processus de Transaction de VitaDAO ? Parmi les projets listés sur leur site, plusieurs chercheurs universitaires ont reçu des subventions d’environ 200 000 à 300 000 dollars.
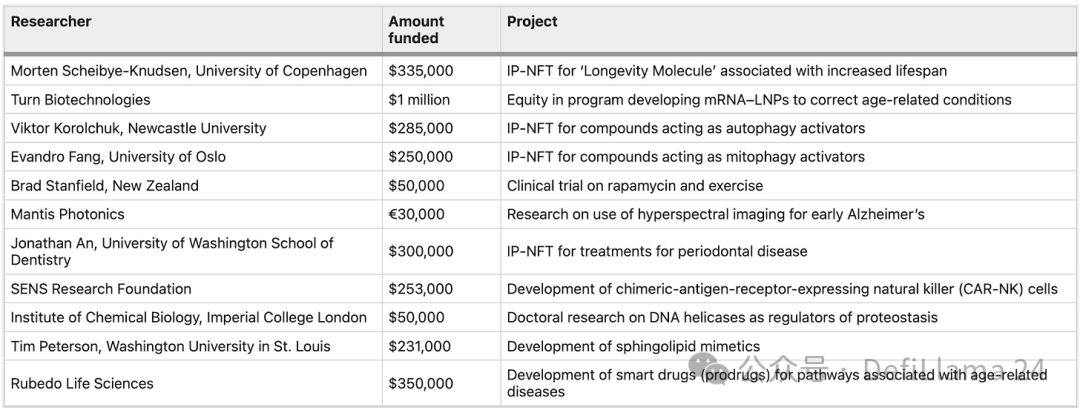
En quoi les chercheurs financés par VitaDAO diffèrent-ils de ceux financés traditionnellement par les NIH ? Prenons le Dr Evandro Fang, dont le projet sur de nouveaux activateurs de mitophagie a récemment reçu un investissement de 300 000 dollars de VitaDAO. Selon son CV, ses travaux ont déjà obtenu plusieurs financements des NIH et d’autres agences gouvernementales. Un autre argument en faveur de la nouveauté de VitaDAO est que leur processus communautaire examine et finance ces projets plus rapidement que les NIH, même si les bénéficiaires se recoupent fortement.
Jusqu’à présent, des initiatives comme Gitcoin ou des organisations comme VitaDAO dans l’écosystème DeSci ont ciblé l’accélération et la simplification du financement de la recherche fondamentale. D’autres projets commencent à s’attaquer aux faiblesses que nous avons soulignées dans l’industrie pharmaceutique, comme le développement de médicaments pour les maladies rares.
Un autre argument précoce en
Bienvenue dans la communauté officielle TechFlow
Groupe Telegram :https://t.me/TechFlowDaily
Compte Twitter officiel :https://x.com/TechFlowPost
Compte Twitter anglais :https://x.com/BlockFlow_News